La osteoartritis (OA) es una enfermedad degenerativa del cartílago articular cuya principal manifestación clínica es el dolor articular. La base de datos del China Health and Retirement Longitudinal Study mostró que la morbilidad de la artrosis sintomática (puntuación de Kellgren y Lawrence de rodilla ≥2, con dolor de rodilla) fue del 8,1% en China. Con el desarrollo del envejecimiento en China, la incidencia de OA está aumentando. Como no hay vasos sanguíneos, nervios o linfa en el cartílago articular, su capacidad de autocuración es deficiente.
Hay muchos tipos de tratamientos no quirúrgicos, como medicamentos que incluyen antiinflamatorios no esteroides, glucocorticoides u opioides, [1,2] así como tratamientos de fisioterapia que incluyen la inyección de ácido hialurónico (HA) o plasma rico en plaquetas (PRP) [3,4] para prevenir el dolor y mejorar la función articular. Todos estos métodos pueden prevenir el dolor temporalmente pero no pueden interrumpir la degeneración del cartílago articular.
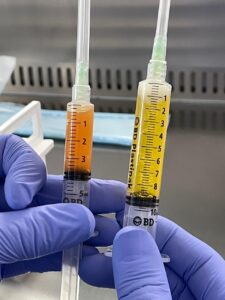
Después de extraer la grasa del cuerpo humano mediante un dispositivo de liposucción, se puede obtener tejido adiposo microfragmentado (MAT) mediante un dispositivo de aislamiento y lavado sin enzimas digestivas. [5] Es compatible con andamios tridimensionales, factores de crecimiento y colonias celulares como las células madre mesenquimales (MSC). La inyección de MAT puede reducir el dolor en pacientes con OA, mejorar la función articular y no causa eventos adversos.
Como tecnología innovadora, la inyección de MAT ha sido certificada por la Administración de Alimentos y Medicamentos (FDA) en los Estados Unidos, la Marca Conformite Europeenne (CE) en Europa y la Administración de Productos Terapéuticos de Australia.
Es simple y seguro, y puede lograr una gran efectividad con una sola inyección, inclusive por encima del 80% de mejoría.
Actualmente se encuentran en curso una gran cantidad de estudios básicos y ensayos clínicos centrados en las inyecciones de MAT en pacientes con lesión del cartílago articular. Según los resultados del seguimiento (incluidos los datos no publicados), la inyección de MAT puede reducir el dolor en los pacientes, mejorar la función articular y no causa eventos adversos. [27]
Incluso en pacientes que se han sometido a muchos tratamientos fallidos, como la cirugía artroscópica del menisco, la reducción del dolor mediante la inyección de MAT es evidente. [24]
Referencias
1. Bellamy N, Campbell J, Robinson V, Gee T, Bourne R, Wells G. Viscosupplementation for the treatment of osteoarthritis of the knee. Cochrane Database Syst Rev 2006; 19:CD005321.doi: 10.1002/14651858.CD005321.pub2. [PubMed] [Google Scholar]
2. Filardo G, Kon E, Longo UG, Madry H, Marchettini P, Marmotti A, et al. Non-surgical treatments for the management of early osteoarthritis. Knee Surg Sports Traumatol Arthrosc 2016; 24:1775–1785. doi: 10.1007/s00167-016-4089-y. [PubMed] [Google Scholar]
3. Kon E, Mandelbaum B, Buda R, Filardo G, Delcogliano M, Timoncini A, et al. Platelet-rich plasma intra-articular injection versus hyaluronic acid viscosupplementation as treatments for cartilage pathology: from early degeneration to osteoarthritis. Arthroscopy 2011; 27:1490–1501. doi: 10.1016/j.arthro.2011.05.011. [PubMed] [Google Scholar]
4. Shen L, Yuan T, Chen S, Xie X, Zhang C. The temporal effect of platelet-rich plasma on pain and physical function in the treatment of knee osteoarthritis: systematic review and meta-analysis of randomized controlled trials. J Orthop Surg Res 2017; 12:16.doi: 10.1186/s13018-017-0521-3. [PMC free article] [PubMed] [Google Scholar]
5. Tremolada C, Colombo V, Ventura C. Adipose tissue and mesenchymal stem cells: state of the art and lipogems(R) technology development. Curr Stem Cell Rep 2016; 2:304–312. doi: 10.1007/s40778-016-0053-5. [PMC free article] [PubMed] [Google Scholar]
6. Vezzani B, Shaw I, Lesme H, Yong L, Khan N, Tremolada C, et al. Higher pericyte content and secretory activity of microfragmented human adipose tissue compared to enzymatically derived stromal vascular fraction. Stem Cells Transl Med 2018; 7:876–886. doi: 10.1002/sctm.18-0051. [PMC free article] [PubMed] [Google Scholar]
7. Zuk PA, Zhu M, Mizuno H, Huang J, Futrell JW, Katz AJ, et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Eng 2001; 7:211–228. doi: 10.1089/107632701300062859. [PubMed] [Google Scholar]
8. Schaffler A, Buchler C. Concise review: adipose tissue-derived stromal cells–basic and clinical implications for novel cell-based therapies. Stem Cells 2007; 25:818–827. doi: 10.1634/stemcells.2006-0589. [PubMed] [Google Scholar]
9. da Silva Meirelles L, Caplan AI, Nardi NB. In search of the in vivo identity of mesenchymal stem cells. Stem Cells 2008; 26:2287–2299. doi: 10.1634/stemcells.2007-1122. [PubMed] [Google Scholar]
10. Schwab KE, Gargett CE. Co-expression of two perivascular cell markers isolates mesenchymal stem-like cells from human endometrium. Hum Reprod 2007; 22:2903–2911. doi: 10.1093/humrep/dem265. [PubMed] [Google Scholar]
11. Corselli M, Chen CW, Sun B, Yap S, Rubin JP, Peault B. The tunica adventitia of human arteries and veins as a source of mesenchymal stem cells. Stem Cells Dev 2012; 21:1299–1308. doi: 10.1089/scd.2011.0200. [PMC free article] [PubMed] [Google Scholar]
12. Hindle P, Khan N, Biant L, Peault B. The infrapatellar fat pad as a source of perivascular stem cells with increased chondrogenic potential for regenerative medicine. Stem Cells Transl Med 2017; 6:77–87. doi: 10.5966/sctm.2016-0040. [PMC free article] [PubMed] [Google Scholar]
13. James AW, Zara JN, Zhang X, Askarinam A, Goyal R, Chiang M, et al. Perivascular stem cells: a prospectively purified mesenchymal stem cell population for bone tissue engineering. Stem Cells Transl Med 2012; 1:510–519. doi: 10.5966/sctm.2012-0002. [PMC free article] [PubMed] [Google Scholar]
14. Zimmerlin L, Donnenberg VS, Rubin JP, Donnenberg AD. Mesenchymal markers on human adipose stem/progenitor cells. Cytometry A 2013; 83:134–140. doi: 10.1002/cyto.a.22227. [PMC free article] [PubMed] [Google Scholar]
15. da Silva Meirelles L, Malta TM, Panepucci RA, da Silva WA., Jr Transcriptomic comparisons between cultured human adipose tissue-derived pericytes and mesenchymal stromal cells. Genom Data 2016; 7:20–25. doi: 10.1016/j.gdata.2015.11.009. [PMC free article] [PubMed] [Google Scholar]
16. Hardy WR, Moldovan NI, Moldovan L, Livak KJ, Datta K, Goswami C, et al. Transcriptional networks in single perivascular cells sorted from human adipose tissue reveal a hierarchy of mesenchymal stem cells. Stem Cells 2017; 35:1273–1289. doi: 10.1002/stem.2599. [PubMed] [Google Scholar]
17. Nava S, Sordi V, Pascucci L, Tremolada C, Ciusani E, Zeira O, et al. Long-lasting anti-inflammatory activity of human microfragmented adipose tissue. Stem Cells Int 2019; 2019:5901479.doi: 10.1155/2019/5901479. [PMC free article] [PubMed] [Google Scholar]
18. Bougle A, Rocheteau P, Hivelin M, Haroche A, Briand D, Tremolada C, et al. Micro-fragmented fat injection reduces sepsis-induced acute inflammatory response in a mouse model. Br J Anaesth 2018; 121:1249–1259. doi: 10.1016/j.bja.2018.03.032. [PubMed] [Google Scholar]
19. Zeira O, Scaccia S, Pettinari L, Ghezzi E, Asiag N, Martinelli L, et al. Intra-articular administration of autologous micro-fragmented adipose tissue in dogs with spontaneous osteoarthritis: safety, feasibility, and clinical outcomes. Stem Cells Trans Med 2018; 7:819–828. doi: 10.1002/sctm.18-0020. [PMC free article] [PubMed] [Google Scholar]
20. Gregory MH, Capito N, Kuroki K, Stoker AM, Cook JL, Sherman SL. A review of translational animal models for knee osteoarthritis. Arthritis 2012; 2012:764621.doi: 10.1155/2012/764621. [PMC free article] [PubMed] [Google Scholar]
21. Hielm-Bjorkman AK, Rita H, Tulamo RM. Psychometric testing of the Helsinki chronic pain index by completion of a questionnaire in Finnish by owners of dogs with chronic signs of pain caused by osteoarthritis. Am J Vet Res 2009; 70:727–734. doi: 10.2460/ajvr.70.6.727. [PubMed] [Google Scholar]
22. Saturveithan C, Premganesh G, Fakhrizzaki S, Mahathir M, Karuna K, Rauf K, et al. Intra-articular hyaluronic acid (HA) and platelet rich plasma (PRP) injection versus hyaluronic acid (HA) injection alone in patients with grade III and IV knee osteoarthritis (OA): a retrospective study on functional outcome. Malays Orthop J 2016; 10:35–40. doi: 10.5704/MOJ.1607.007. [PMC free article] [PubMed] [Google Scholar]
23. Striano RD, Malanga GA, Bilbool N, Azatullah KJJOS, Med S. Refractory shoulder pain with osteoarthritis, and rotator cuff tear, treated with micro-fragmented adipose tissue. Ortho Spine and Sports Med 2018; 2:014. [Google Scholar]
24. Striano R, Chen H, Bilbool N, Azatullah K, Hilado J, Horan KJC. Non-responsive knee pain with osteoarthritis and concurrent meniscal disease treated with autologous microfragmented adipose tissue under continuous ultrasound guidance. CellR4 2015; 3:e1690. [Google Scholar]
25. Franceschini M, Castellaneta C, Mineo GJC. Injection of autologous micro-fragmented adipose tissue for the treatment of post traumatic degenerative lesion of knee cartilage: a case report. CellR4 2016; 1768:4. [Google Scholar].